Wirkungsmechanismus und Prinzipien therapeutischer Wirksamkeit
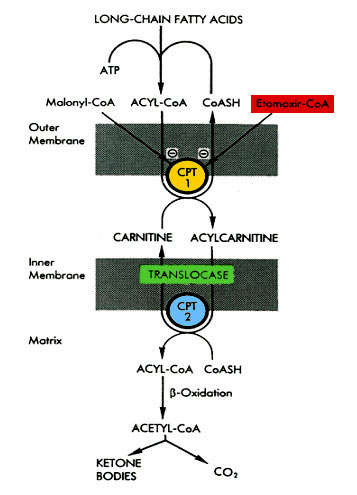
Als Ester wird Etomoxir im Darm zur freien Säure hydrolysiert und wie jede andere Fettsäure absorbiert, transportiert und intrazellulär mit Coenzym A verestert. In dieser Form wirkt Etomoxir als starker Hemmer der mitochondrialen CPT 1 (E.C. 2.3.1.21.). Dieses regulative Enzym ist Bestandteil der äußeren Mitochondrienmembran und katalysiert den Transport der lang-kettigen Fettsäure-CoA –Ester vom Zytosol in die Mitochondrien, in denen der weitere oxidative Abbau stattfindet. Der physiologische Hemmer der CPT 1 ist Malonyl-CoA, ein Metabolit der endogenen Fettsäuresynthese (s. Fig. 1).
Etomoxir-CoA wirkt gewissermaßen als Analogon zu Malonyl-CoA, nur ca. 100 bis 1000 Mal stärker. Dabei ist nur das ( R )-( + )-Isomer wirksamer Hemmer, das (S)-(-)-Isomer ist völlig wirkungslos. Die Hemmung ist, im Kontrast zu der von Malonyl-CoA hervorgerufenen, enzymkinetisch irreversible. Der exakte Mechanismus bleibt noch aufzuklären. In vivo haben wir es mit einer pseudo-reversiblen Hemmung zu tun, da das Enzym rasch nachgebildet wird (s. Lit. 8).
Die Hemmkonzentration, die für eine 50 % ige Hemmung notwendig ist (IC50) wurde in tierischen Geweben zwischen 5 bis 20 nmol/l bestimmt, abhängig vom Organ und metabolischem Zustand (nüchtern, gefüttert, gesund, diabetisch etc.). So ist die in vitro gemessene Sensitivität der CPT 1 in der Rattenleber dieselbe wie im Rattenmuskel (IC50: 6-7 nmol/l). Die Sensitivität des Enzyms im Rattenherzen ist dagegen um den Faktor 2 geringer. Die in vivo Sensitivität nimmt in den untersuchten Rattenorganen wie folgt ab: Leber > Herz > Muskel. Inwieweit die Prozesse des Transportes durch die Zellmembran, der Veresterung mit Coenzym A und des intrazellulären Transportes für diese Unterschiede mit verantwortlich sind, ist noch offen (s. Lit. 79).
Etomoxir hemmt nur die regulative CPT 1, das konstitutionelle Enzym CPT 2 der inneren Mitochondrienmembran, ebenso wie andere Enzyme der β-Oxydation, werden nicht beeinflußt. Dies ist von großer therapeutischer Bedeutung, da z.B. angeborene Defekte dieser Enzyme mit schweren Myopathien einhergehen. Alle beobachteten pharmako-dynamischen Wirkungen des Etomoxirs lassen sich direkt oder indirekt auf die Verschiebung der Energiegewinnung aus Fettsäuren hin zur Energiegewinnung aus Glukose zurückführen. Die verminderte Fettsäureoxydation führt nicht nur zu einer verminderten Ketogenese, Glukoneogenese und Cholesterolsynthese, sondern es wird auch die Insulinresistenz vermindert und über den Mechanismus der Deinhibierung der Pyruvatdehydrogenase kommt es zum Anstieg der Glukoseoxydation.
Die unter der CPT 1 – Hemmung zu beobachtende Erhöhung der Acyl-CoA- konzentrationen im Zytosol führt u.a. zu einer feed-back Hemmung der endogenen Fettsäuresynthese (s. Lit. 82).