
Zusammenfassung
Etomoxir ist der erste Arzneimittelkandidat aus einer neuen Klasse von Substanzen – der Oxirancarbonsäuren – , der in den zwei klinischen Indikationen – Diabetes Typ 2 und Herzinsuffizienz – bis zur klinischen Phase II entwickelt worden ist. Die Substanz hemmt irreversibel die mitochondriale Carnitinpalmitoyltransferase 1 (E.C. 2.3.1.21), ein Enzym, das die Oxydation langkettiger Fettsäuren reguliert. Der wirkliche Hemmer ist der sich intrazellulär bildende Coenzym A – Ester der Substanz.
| INN: | Etomoxir (lat. etomixirum), Ethyl ( + )-2-[6-(parachlorphenoxy)hexyl]glycidat | |
| oder | ||
| ( R )-( + )-2-[6-(4-Chlorphenoxy)hexyl]-oxiran-2-carbonsäure Ethylester | ||
| Summenformel: | C17H23CIO4 | |
| MG: | 326,8 | |
| http://www.dr.wolf-bioscience.de/wp-content/uploads/2016/08/strukturformel-strichmodell.jpg |
Strukturformel:
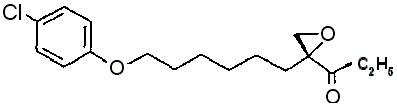
| Indikationen: | Metabolisches Syndrome, Herzinsuffizienz, Diabetes Typ 2, Ketoazidose, Hyperlipidämie, Arteriosklerose, Koronare Herzkrankheit, Entzündungen, Leukämie, Ketose der Milchkuh. | |
| Status: | Phase II der klinischen Entwicklung. | |
| Dosis: | 2 x 40 mg bis 2 x 80 mg täglich. | |
| Arzneiform: | Weichgelatinekapseln | |
| Toxikologie: | Akute Toxizität: (LD50, nüchterne Mäuse, Ratten, p.o.): 270 mg/kg. | |
| Subakute Toxitität: (LD50, Ratte, p.o.): > 125 mg/kg; (LD5, Hund, p.o.): > 200 mg/kg. | ||
| Keine Zeichen von Mutagenität, Embryo - Toxitität und Teratogenität. | ||
